Tenía “la peor infección del planeta” pero su esposa no se dio por vencida hasta salvarlo
Tom Patterson se estaba muriendo a causa de una superbacteria resistente a lo antibióticos. Parecía que no sobreviviría. Pero todo cambió gracias a esposa, que movilizó a expertos hasta encontrar una cura.

Tom y Steffanie con ilustraciones de un Acinetobacter, un tipo de bacterias frecuente en hospitales, y un bacteriófago, virus devorador de bacterias. Crédito: BBC
ADVERTENCIA: el contenido de esta nota puede herir su sensibilidad.
Cuando Tom Patterson comenzó a vomitar durante unas vacaciones en Egipto pensó que era una intoxicación alimentaria. Se equivocaba; había sido infectado con una superbacteria resistente a los antibióticos y solo la determinación de su mujer y un revolucionario tratamiento lograrían salvarlo.
“¿Ya le avisó alguien a Steff de que su marido se va a morir?”
Era una pregunta que se suponía que Steffanie Strathdee no debía escuchar. Había hablado por teléfono con unos colegas, que siguieron conversando entre ellos al pensar que ya había colgado.
Steffanie, una epidemióloga de enfermedades infecciosas, sabía que su marido, Tom Patterson, estaba gravemente enfermo. En esos momentos yacía en un coma médico inducido, pero todavía le resultaba chocante escuchar que se esperaba que falleciera.
“Pensé: ‘Oh, Dios mío. No, nadie ha muerto. Acuné el teléfono entre mis brazos como un bebé y fue un momento muy profundo. Me di cuenta de que si realmente se estaba muriendo yo tenía que hacer algo. Si la medicina moderna no tenía nada que ofrecer, debía poner todo mi empeño”.
Los médicos se estaban quedando sin recursos para mantener vivo a Tom, mientras una superbacteria mortal arrasaba su torrente sanguíneo, resistente a todos los antibióticos que le administraban.
Steffanie había leído en alguna revista médica que a veces la gente en coma puede escuchar, así que decidió pedirle a Tom si quería seguir viviendo.
“Pensé que no podía asumir toda la responsabilidad y mantenerlo con vida si él ya no quería, necesitaba preguntarle”, dice Steffanie.
“Así que sostuve su mano con mi guante azul y le dije: ‘Cariño, si quieres vivir, tienes que dar todo lo que puedas de ti mismo, los médicos ya no tienen más. Todos esos antibióticos no sirven para nada. Así que si quieres vivir, por favor aprieta mi mano y moveré cielo y tierra para conseguirlo”.
Al cabo del rato, Tom apretó mi mano.
“Alcé el puño en el aire y dije: ‘¡Esto es maravilloso!’ Y después me di cuenta: ‘¡Dios mío! ¿Qué voy a hacer ahora? No soy médico, no sé qué hacer'”.
La pareja, ambos científicos de la Universidad de California, en San Diego, se conoció por sus trabajos de investigación de tratamientos contra el sida.
Ávidos viajeros, visitaron juntos unos 50 países.
En noviembre de 2015, se fueron a Egipto. Una bomba terrorista había derribado un avión ruso y debatieron si cancelar el viaje, pero decidieron hacerlo de todos modos.
“Tom dijo: ‘¡Es el momento perfecto para ir, no habrá multitudes!’ Yo le dije: ‘¿Estás loco?’ Pero redacté a mano nuestro testamento y se lo entregué a mis padres. Pensamos que de haber problemas, sería un ataque terrorista o algo así”.
El viaje fue fantástico. La primera parada era el Valle de los Reyes y para llegar allí dieron un paseo nocturno en barco por el río Nilo.
Eran casi los únicos pasajeros en un bote diseñado para 150. Disfrutaron de una maravillosa cena bajo las estrellas en la cubierta del barco, con las aguas del Nilo brillando a su alrededor.
Pero cuando volvieron a su camarote, Tom comenzó a vomitar. Al principio, la pareja asumió que era intoxicación alimentaria. En sus viajes siempre llevaban Cipro, un antibiótico, pero esta vez no funcionó.
Tom siguió sintiéndose peor y comenzó a sentir dolor de espalda.
Steffanie fue con Tom a visitar a unos médicos en tierra firme. Los doctores le hicieron un TAC y descubrieron que no era una intoxicación alimentaria lo que tenía, sino un absceso en su intestino conocido como seudoquiste que había crecido casi hasta alcanzar el tamaño de un balón de fútbol.
Gracias a su seguro médico, que habían comprado por $35 dólares antes de hacer el viaje, Tom fue trasladado en avión a Frankfurt, Alemania, donde los doctores descubrieron que la causa del problema era una piedra expulsada de su vesícula que se había quedado atascada en su conducto biliar.
Dentro del quiste encontraron un líquido marrón oscuro que indicaba que no se trataba de una nueva infección. Mientras trabajaban en averiguar qué era, Tom cayó en coma.
“Yo tenía alucinaciones. Pensaba que estaba en Egipto y veía jeroglíficos en las paredes“, dice Tom. “A causa de la infección en mi intestino -y de que llevaba días sin dormir- me estaba volviendo loco. Los doctores regresaron y dijeron: ‘Esta es la peor infección del planeta, cerró hospitales en Alemania. Se llama Acinetobacter baumannii‘“.
Tom fue puesto en aislamiento y sus hijos volaron a verlo, preocupados al pensar que no sobreviviría. Cuando los médicos le visitaban, se ponían batas especiales.
Eso alarmó a Steffanie, quien conocía los Acinetobacter por sus estudios en microbiología.
“Estaba muy asustada porque es un organismo que solía usar en el laboratorio en los años 80 y entonces era considerado un patógeno muy débil. Solo necesitábamos guantes y una bata de laboratorio, no hacía falta un equipo especial”, dice ella.
“En las dos últimas décadas se ha convertido en un cleptómano bacteriano. Aprendió a robar genes de resistencia a los antibióticos de otras bacterias y adquirió capacidades de superpotencia que lo convirtieron en un patógeno muy mortal“.
En 2017, fue catalogada por la Organización Mundial de la Salud (OMS) como una de las tres superbacterias para la que se necesitan antibióticos con mayor urgencia.
Por suerte, algunos antibióticos funcionaron para Tom, y el equipo médico de Frankfurt pudo estabilizarlo.
Una decisión difícil
Tom y Steffanie eran amigos de varios médicos que pudieron aconsejarles sobre la situación y decidieron volver a San Diego.
Los doctores de Estados Unidos tenían experiencia sobre el Acinetobacter baumanni por la alta presencia de militares en la zona. De hecho, la bacteria había sido apodada“Iraqibacter“ (bacteria iraquí) debido al alto número de infecciones detectadas por las fuerzas estadounidenses en Medio Oriente.
Cuando Tom llegó, volvieron a probar su sensibilidad a los antibióticos. Malas noticia: ninguno de ellos tuvo efectos.
Los médicos tenían que tomar una decisión difícil: podían operarle para extirpar el absceso o tratar de extraer el líquido infectado del cuerpo. Pero decidieron que operarle era demasiado arriesgado: si el organismo penetraba en su torrente sanguíneo, entraría en un shock séptico.
Steffanie describe un shock séptico como una reacción exagerada del sistema inmune del cuerpo al invasor. El cuerpo entra en “alerta roja”, la presión sanguínea disminuye, la frecuencia cardíaca aumenta, la respiración se acelera.
“Ocurre muy rápidamente y tiene una tasa de mortalidad del 50%”, explica ella.
Así que los médicos optaron por sustraer el líquido, introduciendo cinco drenajes en el abdomen de Tom”.
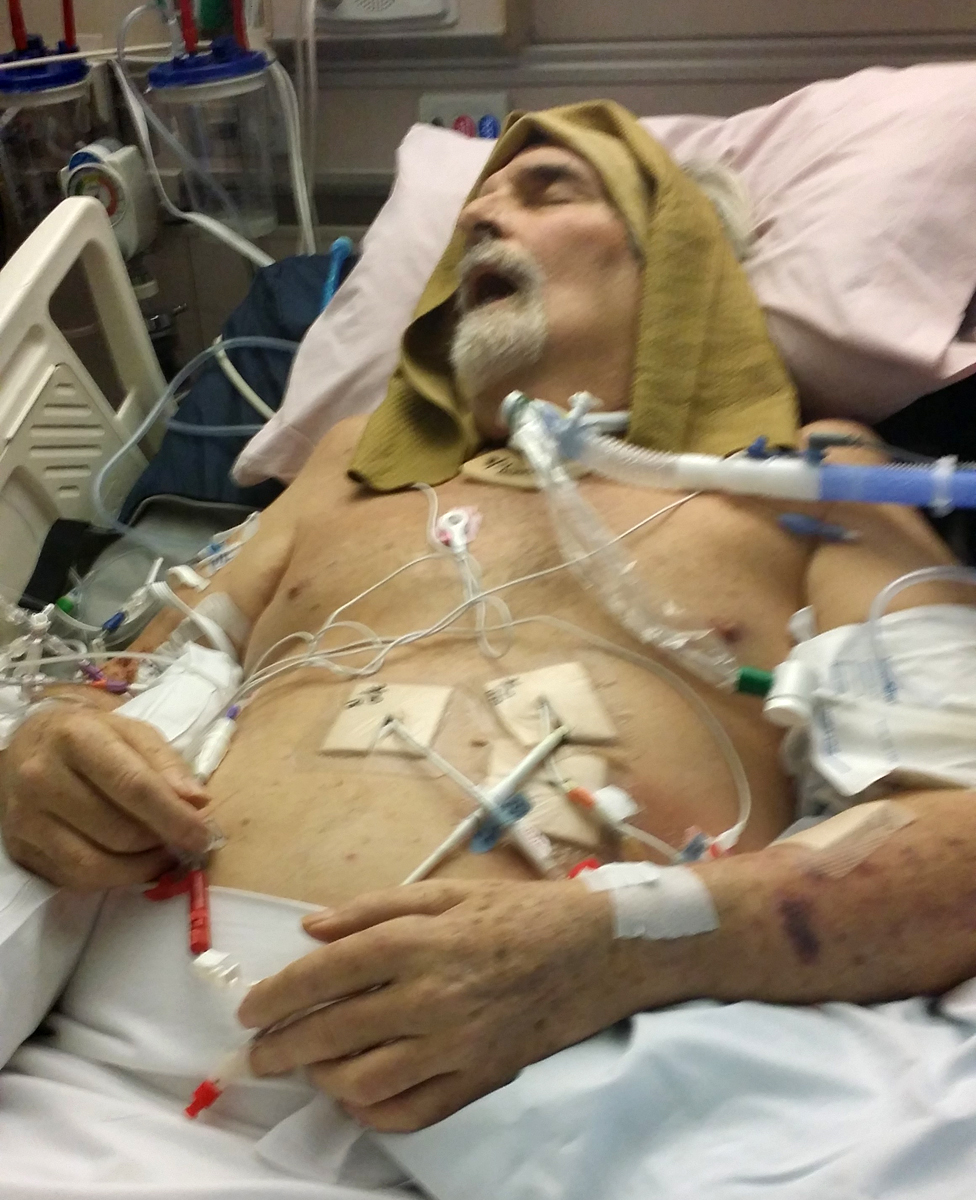
El plan era transferirle a un centro de atención para casos agudos a largo plazo. Sin embargo, un día antes de que eso ocurriera uno de los drenajes se deslizó mientras trataba de sentarse en la cama, vertiendo toda la infección en su torrente sanguíneo.
Inmediatamente, entró en shock séptico, fue trasladado rápidamente a cuidados intensivos y le pusieron un ventilador para respirar.
“A partir de ese momento, la bacteria colonizó todo su cuerpo, estaba en su sangre, no solo su abdomen. Él iba desapareciendo día tras día“, dice Steffanie.
Era un hombre alto, de 1,95 cm, y grande, de 135 kg, y ya había perdido mucho peso.
“Podía colocar mi puño en el hueco de su pómulo y dos nudillos en las órbitas de sus ojos. Era horrible”, dice Steffanie.
En ese punto, Tom no sabía qué estaba pasando. “Estaba alucinando unas elaboradas teorías que eran casi bíblicas. Cosas como que había estado 100 años caminando por el desierto y tratando de responder a tres preguntas planteadas por santos. Eso me sucedió durante días”, dice.
Salió de su coma brevemente y pudo entonces comunicarse con la gente de su alrededor, pero no podía salir de la cama.
Fue entonces cuando Steffanie escuchó a sus colegas preguntar si le habían dicho que Tom se iba a morir, y cuando le pidió que apretara su mano si quería seguir viviendo.
Lo que Steffanie no sabía era que en ese momento él estaba alucinando con que era una serpiente. ¿Cómo podía apretar su mano, si las serpientes no tienen manos? Al final, él se dio cuenta de que podía envolver todo su cuerpo alrededor de la mano de ella, y entonces le dio la señal.
Al darse cuenta de que necesitaban medidas desesperadas, Steffanie consultó PubMed, el sitio de búsqueda de la Biblioteca Nacional de Medicina de Estados Unidos.
“Escribí ‘resistencia a múltiples fármacos’, ‘Acinetobacter baumannii’ y ‘tratamientos alternativos’, y apareció un artículo sobre algo llamado terapia de fagos en el título y pensé: ‘Bacteriófagos … Recuerdo lo que son'”.
Los fagos son virus que evolucionan de manera natural para atacar bacterias y Steffanie los había estudiado durante un tiempo.
Son diminutos, 100 veces más pequeños que las bacterias, y están por todas partes, dice ella: en el agua, en la tierra y en nuestra piel. Se calcula que 30,000 millones de ellos entran y salen de nuestros cuerpos cada día.
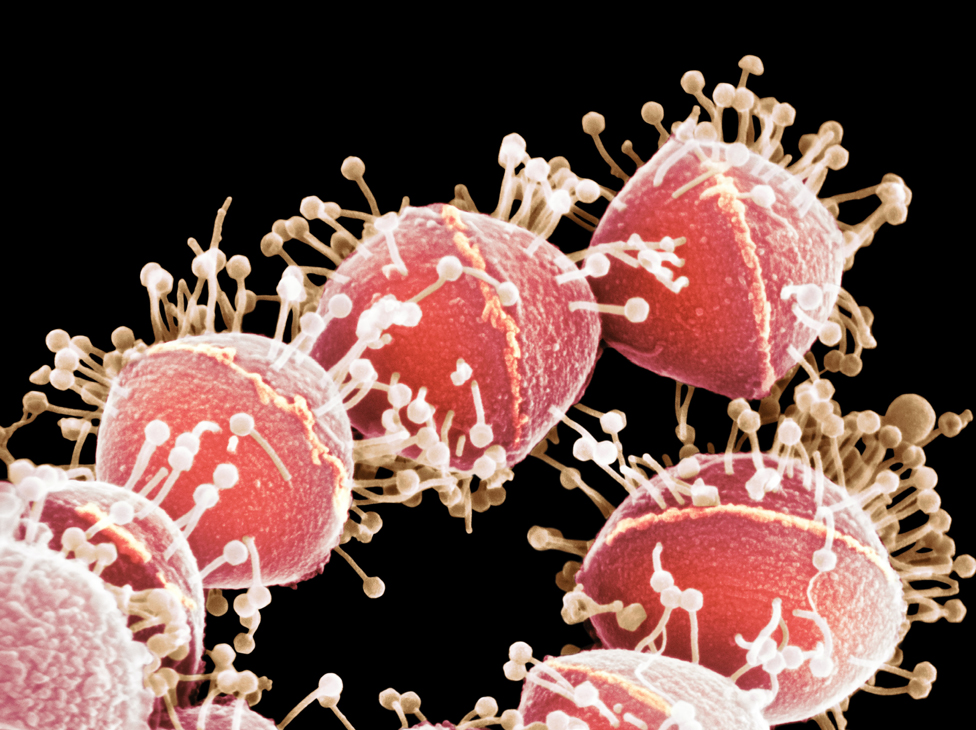
Hace un siglo, los fagos llamaron mucho la atención como una posible cura para las infecciones bacterianas, pero fuera de la antigua Unión Soviética y partes de Europa del Este esta investigación quedó en la cuneta tras el descubrimiento de un maravilloso medicamento, la penicilina, en 1928.
Después de la penicilina llegaron otros tipos de antibióticos, explica Steffanie, que hicieron a los médicos de Occidente pensar que siempre podrían encontrar una cura para cualquier infección bacteriana.
“¡Chico… nos equivocamos!”, suspira ella. “Fue apenas entonces cuando esas superbacterias, esas bacterias que habían sido resistentes a múltiples antibióticos, comenzaron a ser una verdadera amenaza para la salud global y nosotros empezamos a echarles una segunda mirada [a los fagos]”.
Un coctel de virus
El siguiente paso de Steffanie fue acercarse a la Administración de Alimentos y Medicamentos de EE.UU., que había aprobado un tratamiento experimental por razones humanitarias.
Pero había un obstáculo. Para que el tratamiento funcionara, Steffanie tenía que encontrar fagos que coincidieran con el tipo particular de bacteria Acinetobacter con la que Tom estaba infectado… y con los billones de fagos que hay en el planeta, no era tarea fácil.
Steffanie volvió a consultar internet y contactó a investigadores en Norteamérica que esperaba que le pudieran ayudar, aunque ninguno estaba usando fagos como tratamiento médico.
El doctor Ry Young, de la Universidad de Texas A&M, le respondió rápidamente, ofreciéndose a convertir su laboratorio en un centro de mando y pidiendo a expertos en fagos de todo el mundo que le enviaran sus fagos para probarlos contra la bacteria de Tom.
“Teníamos especialistas de todo el mundo ofreciendo su ayuda, desde Suiza y Bélgica hasta Polonia, Georgia o India. Los belgas incluso ofrecieron enviar su fago en una valija diplomática. Eran completos desconocidos que habían asumido el reto, una verdadera aldea global para rescatar a un hombre”, dice Steffanie.
En tres semanas, gracias en parte a un estudiante de doctorado que dormía en el laboratorio, trabajando día y noche, prepararon un coctel de cuatro fagos.
En ese punto, Tom estaba conectado a un respirador artificial. Sus pulmones y sus riñones estaban fallando, usaba un ventilador y necesitaba tres medicamentos diferentes para mantener su corazón latiendo.
Puede que estuviera tan solo a unas horas de morir.
La atmósfera en el hospital era emocional, casi espiritual.
“La gente encendía velas, decía plegarias, enviaba recomendaciones de canciones. Teníamos música sonando de fondo y Tom incluso recuerda que los Beatles sonaban cuando entraba y salía del coma”, cuenta Steffanie.
La responsabilidad del tratamiento experimental caía fuertemente sobre sus hombros.
“Era aterrador porque pensé: ‘Bueno, va a a morir de todos modos si no hacemos esto… pero si esto le mata, pesará en mi conciencia el resto de mi vida'”.
El primer coctel de fagos se inyectó en tubos en el abdomen de Tom, el más cercano a la infección. Cuando estaba más estable, se inyectó en su torrente sanguíneo un segundo y más potente cóctel de fagos, desarrollado en un centro médico de la Marina estadounidense.
Era una verdadera innovación, pues incluso en sitios donde se usa la terapia de fagos no suele administrarse de manera intravenosa.
Los preparados de fago podrían matar al paciente si no estaban lo suficientemente limpios, y a menudo provienen de lugares oscuros ricos en bacterias como alcantarillas, “de algunos de los lugares más peligrosos que puedas imaginar”, según dice Steffanie.
Pero tres días después de que le administraran el coctel de fagos, Tom despertó del coma.
“Mi hija estaba de pie, a mi lado, tomé su mano y la besé”, dice él. “No podía hablar en ese momento y estaba muy cansado. Me volví a dormir”.

Poco después del comienzo de la terapia con fagos, Tom tuvo otro caso de shock séptico, su sexto de siete en total durante los nueve meses que pasó en el hospital.
Usaron varios fagos mientras continuaba su tratamiento, y la bacteria desarrolló resistencia a algunos de ellos. No está completamente claro qué fagos funcionaron y cuáles no.
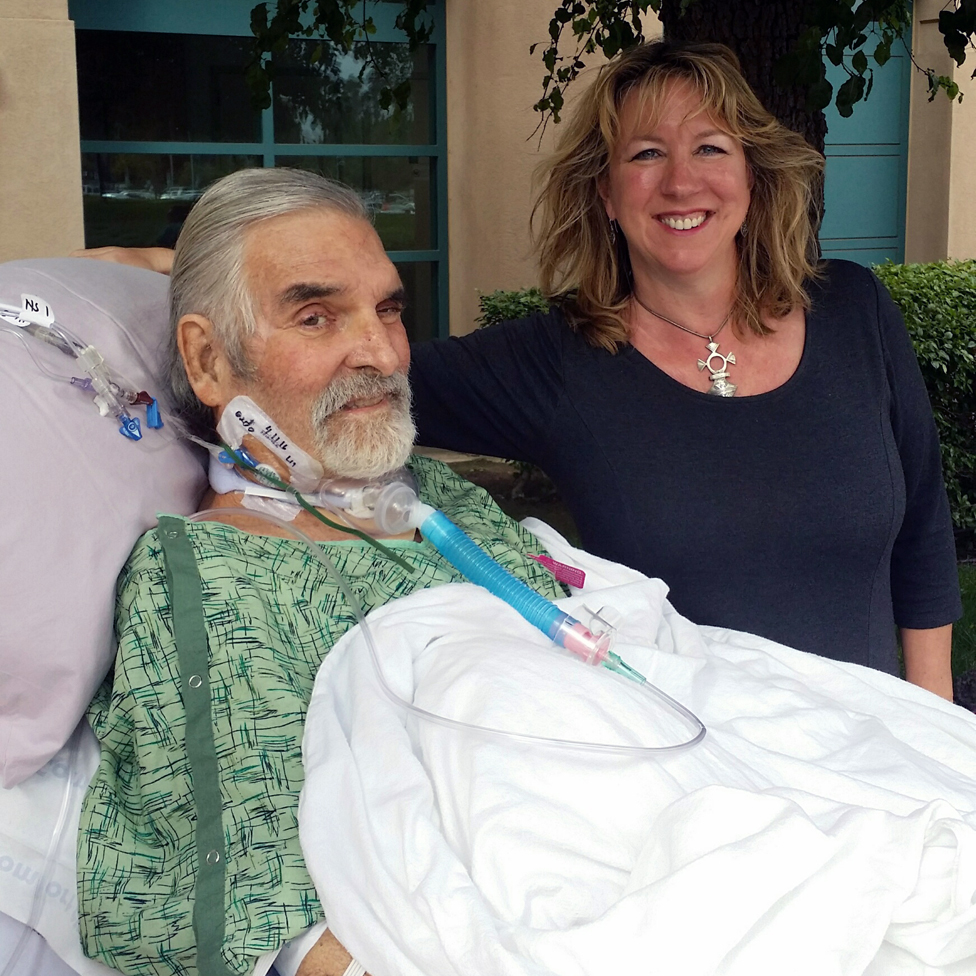
Ahora está en las tres cuartas partes del recorrido a una recuperación que se prevé dure cuatro años.
Tuvo que aprender de nuevo a tragar, a caminar, a ponerse de pie. Salió del hospital en silla de ruedas porque sus músculos no respondían.
Una de las lecciones que recuerda Tom de sus meses en el hospital es la importancia de la compañía.
Su yerno organizó un horario de visitas para asegurarse de que alguien estuviera con él las 24 horas del día, los 7 días de la semana, e incluso cuando estaba en coma, a menudo podía escuchar, en la distancia, lo que sucedía.
“Podía escuchar a la gente hablando, me leían y cantaban, y me tomaban de la mano, y un toque era como una descarga eléctrica, mucha energía viniendo hacia ti”, dice.
Tom fue la primera persona en Norteamérica en recibir terapia de fagos por vía intravenosa para tratar una infección sistemática con superbacterias.
Steffanie reconoce lo afortunados que fueron y cuánto dependieron de sus contactos, que le permitieron lanzar la campaña internacional para salvar a su esposo.
Cuando, un año después de la recuperación de Tom, su caso fue presentado en el Instituto Pasteur de París, en una reunión para conmemorar el centenario del descubrimiento del bacteriófago en 1917, Steffanie comenzó a recibir llamadas de personas de todo el mundo, cuyos familiares estaban muriendo por infecciones de superbacterias y que querían probar la terapia con fagos.
“Estaba abrumada”, dice ella. “Pero intenté tener el mismo tipo de respuesta que recibí para Tom. Salvamos a algunas personas, no solo sus vidas sino sus extremidades, y uno de los casos más milagrosos fue el de Isabelle”.
Isabelle Carnell-Holdaway, una adolescente británica que padece fibrosis quística, había desarrollado una infección resistente a los antibióticos tras un trasplante de pulmón. Pudo recuperarse con una terapia de fagos desarrollada por un equipo liderado por el doctor Chip Schooley, el médico responsable del tratamiento de Tom.
En cuestión de meses recuperó la rutina, a pesar de que le habían dado un 1% de posibilidades de supervivencia.
No obstante, todavía hay muchos obstáculos para que la terapia con fagos forme parte de la medicina convencional.
Los fagos no son como los medicamentos, que pueden servir contra una amplia variedad de organismos. Los fagos funcionan mejor cuando se adaptan con mucha precisión a la bacteria de cada paciente, lo que hace que su diseño sea más complejo. Hasta ahora ha habido pocos ensayos clínicos.
Pero Steffanie y Tom se han convertido en evangelistas de los fagos.
Contaron su historia en un libro The Perfect Predator (“El depredador perfecto”), que ahora se está convirtiendo en un documental y en una película de Hollywood.

También abrieron el Centro para la Terapia de Fagos Innovadora y Terapéutica de la Universidad de California, el primer centro dedicado de terapia de fagos en América del Norte.
Parte de su misión es concienciar a la gente sobre la urgencia de encontrar una solución a la resistencia a los antibióticos.
A menos de que se haga algo, dice Steffanie, una persona morirá de una infección por superbacterias cada tres segundos hacia 2050.
“Como epidemióloga de enfermedades infecciosas, tener a mi esposo muriendo por una superbacteria era muy impactante”, dice Steffanie.
“Era como una broma cruel de Dios. Una parte de mí era la científica que trataba de analizar las cosas y de tomar el control; la otra parte era la esposa tratando de tomar la mano de su esposo y hacer frente a una situación desesperada”.
“Pero, para ser honesta, me avergonzó haber estado tan ciega ante esta amenaza global, la crisis de las superbacterias, que me había invadido”.
- FOTOS: Se hizo una manicura y contrajo una bacteria come-carne en el pulgar
- La amenaza bacteriana que puede matar a 10 millones de personas cada año
Todas las imágenes son cortesía de Steffanie Strathdee.
Ahora puedes recibir notificaciones de BBC Mundo. Descarga la nueva versión de nuestra app y actívalas para no perderte nuestro mejor contenido.
https://www.youtube.com/watch?v=obfMLsimdy8




